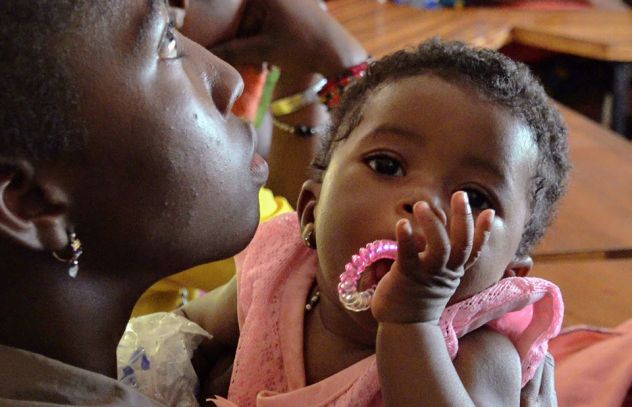
Menos del 60% de las mujeres embarazadas que viven con el VIH en África occidental y central tienen acceso a servicios para detener la transmisión vertical del VIH.
19 DE ABRIL DE 2021
Ha habido éxitos en el compromiso de poner fin a la transmisión vertical del VIH (de madre a hijo). Por ejemplo, en África oriental y meridional, el 95% de las mujeres embarazadas que viven con el VIH recibieron terapia antirretroviral para prevenir la transmisión vertical del VIH en 2019.
Sin embargo, tales éxitos no se han visto de forma universal. En África occidental y central, el panorama no es tan positivo: la cobertura de servicios para la prevención de la transmisión vertical en la región se encuentra entre las más bajas del mundo. En 2019, solo el 58% de las mujeres embarazadas que viven con el VIH en la región recibieron terapia antirretroviral para prevenir la transmisión vertical.
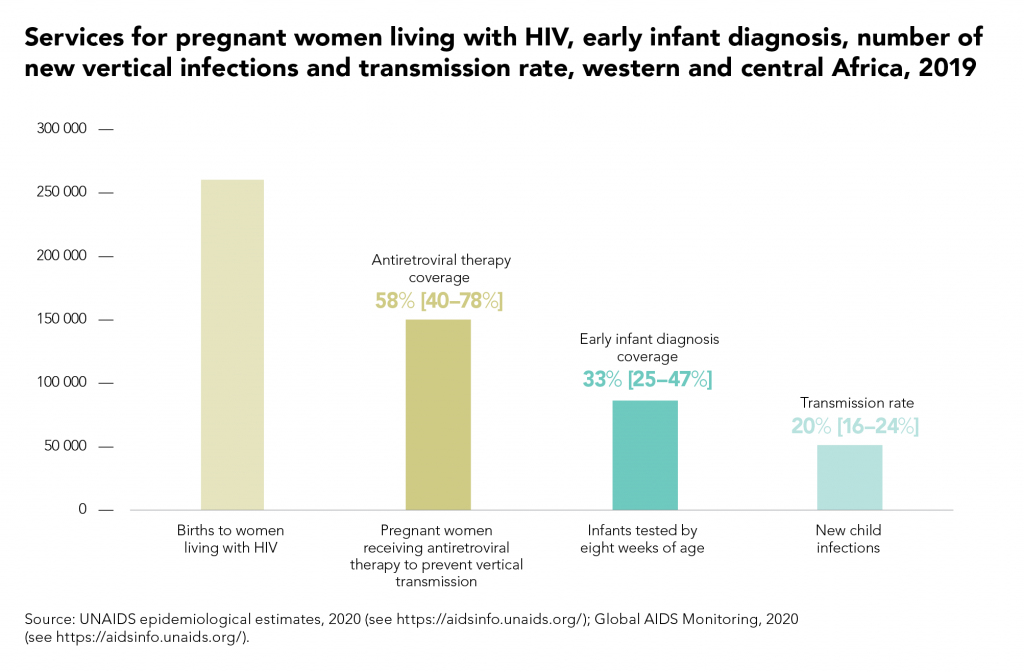

CROI 2021: Los tratamientos antirretrovirales confirman su eficacia en la prevención de la transmisión vertical del VIH
Además, un estudio realizado en África confirma la recomendación de dolutegravir como tratamiento seguro y eficaz para mujeres embarazadas con el VIH
El uso de dolutegravir y de efavirenz resulta seguro y eficaz tanto para las mujeres embarazadas con el VIH como para
sus hijos, según los datos del ensayo DolPHIN-2, presentados en la Conferencia sobre Retrovirus e Infecciones Oportunistas (CROI), celebrada recientemente de forma virtual debido a la pandemia de la COVID-19.
En 2019, la Organización Mundial de la Salud (OMS) recomendó el uso de dolutegravir (Tivicay®, también en Triumeq® y Dovato®) como parte del tratamiento antirretroviral para las mujeres con el VIH embarazadas (véase La Noticia del Día 25-07-19). Hasta la fecha el tratamiento estándar de esta población estaba basado en efavirenz (Sustiva® o Stocrin®, también en Atripla® y Symfi®). Estas nuevas directrices venían a resolver las dudas sobre si las mujeres en edad fértil deberían tomar o no dolutegravir dado que el año anterior en el estudio de Tsepamo (Botsuana) se detectó un aumento en la tasa de defectos del tubo neural en bebés que estuvieron expuestos al fármaco en torno al momento de la concepción y las primeras fases del embarazo (véase La Noticia del Día 22/05/2018).
El estudio DolPHIN-2 se diseñó con el fin de comparar la eficacia de dolutegravir, respecto a la de efavirenz, a la hora de controlar la carga viral del VIH en mujeres que empezaron el tratamiento al final del embarazo. Es importante que la mujer alcance la carga viral indetectable lo antes posible para prevenir la transmisión del VIH de madre a hijo. En la edición del año pasado de la CROI ya se había informado de los hallazgos de dicho ensayo que revelaban que, en el momento del parto, había más mujeres con carga viral indetectable en el grupo que recibía dolutegravir más dos inhibidores de la transcriptasa inversa análogos de nucleósido/nucleótido (ITIN) que en el grupo asignado para recibir efavirenz. Además, el número de bebes que adquirieron el VIH fue mayor en el brazo de efavirenz que en el de dolutegravir.
Con relación a este tema, el Plan de Emergencia del Presidente de EE UU para Paliar el Sida (PEPFAR, en sus siglas en inglés) indicó en 2019 en la revista Medscape Medical News que 1 millón de personas abandonaba el tratamiento con efavirenz debido a distintos efectos secundarios como la fatiga o la depresión. Esto podría suponer una dificultad para mantener una carga viral indetectable y, junto con la posibilidad de adquirir el VIH en caso de no tenerlo, hace difícil el periodo posparto para las mujeres.
En esta edición de la conferencia, se han presentado los resultados del estudio DolPHIN-2 hasta 18 meses después del parto, procedentes de una cohorte de 250 mujeres con el VIH en Uganda y Sudáfrica que amamantaron a sus bebes durante seis meses sin el uso de leche maternizada y luego continuaron amamantándolos de forma no exclusiva de seis a un año. La edad media de las participantes fue de 28 años (siendo la edad de 18 años el mínimo para poder ingresar al estudio). Las mujeres entraron en el ensayo cuando ya se encontraban, de mediana, en su semana 31 de embarazo, es decir, en el tercer trimestre de gestación. Solo para el 12% era su primer embarazo mientras que las demás habían dado a luz a un promedio de dos hijos previamente.
En el momento de entrar en el estudio, ninguna de las participantes estaba recibiendo tratamiento para su infección por el VIH y la mediana de su recuento de CD4 era de 449 células/mm3. La carga viral media encontrada en este estudio fue mucho mayor a las 1000 copias/mL, umbral por debajo del cual el riesgo de transmisión vertical del VIH disminuye significativamente.
Las mujeres fueron distribuidas de forma aleatoria para recibir un tratamiento antirretroviral que contenía dolutegravir o efavirenz. Los investigadores encontraron que las mujeres incluidas en el primer grupo alcanzaron el umbral de carga viral de 1000 copias/mL en una semana y un nivel indetectable en una mediana de 4,14 semanas. En el brazo de efavirenz las mujeres tardaron 3,71 semanas en bajar de 1000 copias/mL en su carga viral y 12 semanas en alcanzar la indetectabilidad. En otras palabras, las mujeres que tomaban dolutegravir fueron un 83% más rápidas en alcanzar una carga viral inferior a 100 copias/mL y un 93% más rápidas en tener la carga viral indetectable que aquellas mujeres que tomaban un tratamiento basado en efavirenz.
Aunque ambos regímenes fueron efectivos para prevenir el rebote de la carga viral, en el brazo de mujeres con efavirenz hubo ocho mujeres que experimentaron un fracaso en su tratamiento, frente a tres en el de dolutegravir. De este total de 11 mujeres, seis no tenían una carga viral indetectable a la semana 24 y cinco vieron como su carga viral volvía a subir tras haber alcanzado la indetectabilidad. Por otro lado, a la semana 72, el perfil de tolerancia de los dos fármacos era bueno. En total, se registraron 57 eventos adversos, 49 de ellos graves, aunque solo el 3% de ellos estuvieron relacionados con el fármaco, tres en el brazo de dolutegravir y cinco en el de efavirenz.
El 56% de los bebés (136 de 242) experimentaron algún efecto secundario y uno de cada cuatro de ellos fue grave, siendo los más destacados las hernias umbilicales y las marcas de nacimiento. Sin embargo, en ninguno de los casos fueron vinculados a los antirretrovirales. Se registró el fallecimiento de once bebés, ocho de ellos en el brazo de dolutegravir.
Solo hubo un caso de infección por el VIH en un bebé cuya madre estaba tomando efavirenz. El bebé dio positivo al finalizar a las 72 semanas el estudio, pero con anterioridad había dado negativo al nacer, a las seis semanas y a las 12 (no realizó las visitas programadas a las semanas 24 y 48). Aun así, la madre sí recibió seguimiento de forma constante y se sabe que tenía un nivel de carga viral bajo (aunque detectable) en el momento del parto (126 copias/mL) y a la semana 12 (69 copias/mL). El resto de semanas sí mantuvo un nivel indetectable de carga viral indetectable, excepto a la semana 24, en que se produjo un repunte temporal de la carga viral (blip), llegando a 126 copias/mL.
Respecto a este caso, el equipo de investigadores ha informado que, aunque la madre se encontrara por debajo del ya mencionado límite de 1000 copias/mL, la viremia de madre e hijo presenta un patrón similar de resistencia a los medicamentos, lo que apuntaría a que efectivamente el VIH del bebé está vinculado con el de la madre, aunque aún no se ha realizado un análisis filogenético más profundo para confirmarlo.
En sus conclusiones, los autores indican que los datos siguen respaldando las recomendaciones de tratamiento de la OMS sobre el uso de dolutegravir en el embarazo dado que tiene una eficacia virológica superior, una rápida supresión de la carga viral tras el inicio del tratamiento y que esta se mantiene durante todo el período de lactancia. En el caso de efavirenz, a pesar de tener evidencias de supresión virológica, destacan el potencial de transmisión durante la lactancia materna.
Fuente: (gTt-VIH) Grupo De Trabajo Sobre Tratamientos del Vih http://gtt-vih.org
Fuente: ONUSIDA https://www.unaids.org/es
